Cosméticos e alimentos “sem química” são feitos de antimatéria?
Esteban Lopez Moreno
Professor Associado na Fundação Cecierj, membro do Programa HCTE/UFRJ
Quando lecionamos em sala de aula, os alunos tendem a acreditar que o professor detém todo o conhecimento do que está expondo ou pelo menos o principal e que ele terá a resposta infalível para todas as dúvidas. Mas eis que surge aquela pergunta desconcertante que atinge em cheio o docente ou aquela indagação que aparenta não ter qualquer sentido e que se revela cheia de surpresas. A pergunta que intitula este artigo é uma delas e faz parte de uma série de tentativas bem-humoradas de relacionar alguns dos encontros e desencontros da Química com o dia a dia. Sua inspiração começou como gracejos com os alunos e entre colegas professores, que por sua vez acabaram por também contribuir com novas e divertidas indagações. Com o tempo, percebemos que, além de cativar o interesse, elas possuem potencial educativo, que pode ser explorado em sala de aula.
A abordagem, na verdade, não é original. Livros como Por que os homens têm tetas? (Ed. Planeta) ou E se?: Respostas científicas para perguntas absurdas (Companhia das Letras), ambos best sellers, baseiam-se na mesma estratégia de divertir e instruir com perguntas científicas curiosas e inquiridoras. O reconhecimento do “problema” é o ponto central da aprendizagem e, como tal, pode ser utilizado em diferentes metodologias, como PBL, problematização e método de caso.
Ao tentar responder às 14 perguntas, todas relacionadas à Química, é proposto um desafio ao mesmo tempo criativo e educativo, entretanto sem qualquer pretensão de encontrar uma resposta correta. A seguir apresento algumas propostas para respondê-las. Elas não trazem o mesmo rigor que um texto acadêmico, não obstante certamente forneçam boas inspirações e provocações. Recomendamos tentar responder às perguntas antes de ler as respostas. E boa sorte!
- Já que dizem que a água com pH básico favorece a saúde, por que não lhe adicionar um pouco de soda cáustica?
- Qual a diferença entre o “homem de ferro” e o “homem de aço”, além da adição de 0,5 a 1,7% de carbono? (Obs.: o que torna o ferro diferente do aço é o teor de carbono).
- Quando duas pessoas reagem entre si, elas liberam ou absorvem calor?
- Uma molécula orgânica saturada parece dizer que está de mau humor; então ela não deveria reagir com maior facilidade do que as insaturadas?
- Uma solução básica precisa renovar o seu modelito?
- Se um mol de qualquer substância tem 6,02 x 1023 moléculas e cada qual precisasse de um segundo para ser contabilizada, isso quer dizer que demandaria 1,9 x 1016 anos, i.e., 19.000.000.000.000.000 anos, anterior à existência da Terra e do próprio universo?
- Os “radicais livres” são os extremistas ideológicos da Química?
- Cosméticos e alimentos “sem química” são feitos de antimatéria?
- Quando rola uma química entre duas pessoas, forma-se uma ligação de Van der Waals ou de Hidrogênio?
- O poço de Lennard-Jones é onde se encontram os químicos deprimidos?
- Se uma das possíveis origens da palavra “Química” remonta ao leito fértil do Rio Nilo, não seria mais justo, de acordo com o imaginário popular depreciativo da química, associá-la ao Rio Tietê?
- Por que a constante universal de “gases” (R) também se aplica aos líquidos (na equação de entropia estatística de Boltzmann) ou mesmo para o fluxo elétrico (na equação de Nernst)?
- Se boa parte dos átomos e moléculas que compõem a nossa atmosfera continua presente no ambiente desde épocas pregressas, quer dizer que eventualmente posso inalar um “pum” do Hitler ou o dióxido de carbono exalado por Madre Teresa de Calcutá?
- Uma vez que os diamantes são eternos e o carvão é o seu alótropo mais estável termodinamicamente, as joias não deveriam ser feitas com pedaços de carvão?
- Já que dizem que a água com pH básico favorece a saúde, por que não lhe adicionar um pouco de soda cáustica?
- Qual a diferença entre o “homem de ferro” e o “homem de aço”, além da adição de 0,5 a 1,7% de carbono? (o que torna o ferro diferente do aço é o teor de carbono).
- Quando duas pessoas reagem entre si, elas liberam ou absorvem calor?
- A água mineral é um minério?
- Uma solução básica precisa renovar o seu modelito?
- Se um mol de qualquer substância tem 6,02 x 1023 moléculas e cada qual precisasse de um segundo para ser contabilizada, isso quer dizer que demandaria 1,9 x 1016 anos, i.e., 19.000.000.000.000.000 anos, anterior à existência da Terra e do próprio universo?
- Uma simples gota d’água contém dois sextilhões de átomos de oxigênio (2 x 1021 ou 2 seguido de 21 zeros) e o dobro de hidrogênios.
- Uma partícula de poeira contém cerca de três trilhões (ou 3 x 1021) átomos.
- Uma típica célula humana contém aproximadamente 100 trilhões de átomos. O vírus da AIDS tem 800 átomos de carbono de espessura e contém aproximadamente 100 milhões de átomos ao todo.
- O número de átomos em 12 gramas de carvão (i.e., aproximadamente 6 x 1023) é mais do que 1.400.000 vezes maior que a idade do universo em segundos.
- Os “radicais livres” são os extremistas ideológicos da Química?
- Cosméticos e alimentos “sem química” são feitos de antimatéria?
- Quando rola uma química entre duas pessoas, forma-se uma ligação de Van der Waals ou de hidrogênio?
- O poço de Lennard-Jones é onde se encontram os químicos deprimidos?
- Se uma das possíveis origens da palavra Química remonta ao leito fértil do Rio Nilo, não seria mais justo, de acordo com o imaginário popular depreciativo da Química, associá-la ao Rio Tietê?
- Por que a constante universal de “gases” (R) também se aplica aos líquidos (na equação de entropia estatística de Boltzmann), ou mesmo para o fluxo elétrico (na equação de Nernst)?
- Se boa parte dos átomos e moléculas que compõem a nossa atmosfera continua presente no ambiente desde épocas pregressas, quer dizer que eventualmente posso inalar um “pum” do Hitler ou o dióxido de carbono exalado por Madre Teresa de Calcutá?
- Uma vez que os diamantes são eternos e o carvão é o seu alótropo mais estável termodinamicamente, as joias não deveriam ser feitas com pedaços de carvão?
R. Parece um gracejo, mas é uma proposta pertinente; podemos facilmente adicionar um pouco de hidróxido à água para deixá-la alcalina. Não significa que beber água com pH ligeiramente básico ou ácido venha a fazer qualquer diferença para o organismo, pois rapidamente o estômago – rico em ácido clorídrico – encarrega-se de acidificá-la, tornando qualquer leve basicidade inócua. Aliás, todos os órgãos do corpo têm seus próprios mecanismos de regulação do pH – a homeostase –; não fosse isso, você e eu não estaríamos lendo este texto. Os únicos beneficiários da moda de ingestão de água básica são os fabricantes de equipamentos de alcalinização (e não são baratos!), além de alguns médicos desinformados e seus séquitos (Moreno, 2018).
Cabe uma importante ressalva: a adição de qualquer substância alcalina na água, especialmente uma base forte, como a soda cáustica, requer a ajuda de um químico ou profissional competente.
R. Há uma longa história por trás dessa pergunta. A produção do ferro foi um dos marcos mais importantes da evolução de nossa espécie. Em função da facilidade de acesso e aos avanços de sua metalurgia, as novas ferramentas tornaram-se gradualmente mais baratas e eficientes do que as de bronze e equiparam o ser humano para um maior controle da natureza e domínio de outros povos. Os primeiros artefatos constituídos de ferro terrestre datam de cerca de 2000 a.C. e, com a inventividade humana, descobriu-se que a adição de pequenas quantidades de carbono, originalmente provenientes de óleo ou sangue (animal ou humano, geralmente de escravizados), aumentava a rigidez do material, apesar de comprometer o seu brilho. Com o tempo descobriu-se que a concentração ideal estava entre 0,5 a 1,7% de carbono, e passou-se a usar como fonte o próprio carvão das fornalhas.
A metalurgia do ferro tornou-se um conhecimento essencial e muito venerado. Diversos deuses ferreiros passaram a fazer parte do panteão das principais mitologias, como o deus grego Hefesto ou a sua versão romana Vulcano, que também se tornou o patrono da alquimia. Havia ainda o Huracán entre os antigos maias ou o nórdico Thor – o verdadeiro, não esse profiteroles da Marvel Studios –, entre outros, cada qual com suas nuances e historicidade.
Segundo o historiador Mircea Eliade, “o ferro ainda hoje conserva o seu extraordinário prestígio mágico-religioso, mesmo entre os povos que possuem uma história cultural bastante avançada e complexa” (Eliade, 1979). Não por menos, nomes como homem de ferro ou homem de aço são lembranças atávicas de parte desse imaginário antigo, que também resvalam em termos modernos, tais como: “cortina de ferro”, “punho de ferro”, “testa de ferro”, “dama de ferro” (um dos epítetos da primeira-ministra inglesa Margaret Thatcher), "Iron Maiden" (grupo de hard rock), Stálin (i.e. “feito de aço”) etc.
Nas histórias de super-heróis, contudo, o ferro já perdeu, ao menos em parte, o seu prestígio. No blockbuster Homem de Ferro II, o próprio herói informa que sua armadura, contrastando com o nome do herói, é feita de tungstênio. Por que não chamá-lo de “Homem de Tungstênio” ou “Homem de Wolfrâmio”, conforme esse elemento é também conhecido? E ainda teria um significado peculiar mais rico, Wolfrâmio pertence ao imaginário alquímico e significa “lobo devorador”. Seria uma ótima combinação do Wolverine e o Homem de Lata do Mágico de Oz.
R. Essa é a famosa “química” que se diz rolar nos relacionamentos bem-sucedidos e uma das poucas metáforas benfazejas de nossa querida ciência. Sim, deve liberar mais calor, pois o organismo é incitado a produzir, por exemplo, hormônios, como adrenalina, dopamina, feniletilamina, oxitocina. Relacionamentos calorosos estimulam também nossa atividade cerebral, gerando mais tempo e intensidade de gasto energético. Por outro lado, receber aquele “gelo”' em uma relação, sendo ignorado por algum ente querido, pode conduzir à depressão e à diminuição da atividade física; consequentemente, da atividade metabólica. São especulações, mas fazem sentido, não?!
R. Não, a água só é considerada um minério em estado sólido, i.e., gelo. A água mineral recebe esse nome por ter sido obtida a partir de recursos de mineralogia, como perfuração, sondagem etc., da mesma forma que o petróleo é um recurso mineral, não um minério.
Existe muita desinformação sobre o que é um minério. Se pesquisarmos no Google ou em nossos livros didáticos, veremos que algumas definições não condizem com as normas oficiais, como relacionar o minério a uma estrutura cristalina ordenada – em geral contendo compostos inorgânicos em estado sólido – ou ainda fazer parte da crosta terrestre por processos geológicos. Frequentemente sim, mas o âmbar é orgânico, o mercúrio é líquido e ambos não possuem estrutura cristalina ordenada; não obstante, são considerados minerais. Quanto à origem, há os minérios de origem extraterrestre encontrados em bólidos que caem diariamente em nosso planeta, além daqueles que se formam dentro de seres vivos, como a calcita, além do oxalato de cálcio e do fosfato de cálcio – que compõem as temíveis e dolorosas pedras nos rins. Há também os mineraloides, como a opala e a obsidiana, que possuem uma estrutura cristalina disforme.
Existem, portanto, muitas nuances e exceções, e isso tem alterado a definição de minério ao longo do tempo. Por isso, hoje em dia costuma-se colocar em seu conceito algo como “geralmente”; assim, amenizam-se as ressalvas.
Quando trabalhei no Centro de Tecnologia Mineral (Cetem), dizia-se que a Mineralogia é como uma Química “suja”. Faz pleno sentido, na medida em que constatamos que seus principais entes de pesquisa, os minérios, estão cheios de impurezas – diferente de nossos frascos de substâncias, geralmente com o grau PA (para análise), que chegam facilmente a mais de 99,9% de pureza. A incerteza está também em sua estrutura. Os cristais de minérios têm, em maioria, estruturas imperfeitas, algumas bastante caóticas, uma vez que o seu crescimento é limitado por uma miríade de outros cristais que se formam nas proximidades.
Toda essa subjetividade é devidamente organizada pela International Mineralogical Association (IMA), um órgão internacional, semelhante à nossa IUPAC, que regula a definição e a nomenclatura das espécies minerais. A IMA possui, em 2021, 5.571 minérios oficialmente catalogados e reconhecidos; entretanto, há ainda 5.930 em análise ou tratados não oficialmente como minérios. Boa parte do rico catálogo da IMA está disponível neste endereço: https://rruff.info/ima/. Outra ótima opção é o Mindata: https://www.mindat.org/.
R. Não deixa de fazer sentido. A palavra “base”, mesmo na Química, veio incorporada ao conceito de acidez muito tardiamente; os ácidos sempre tiveram o protagonismo, não obstante a importância ser a mesma. Ainda hoje ninguém usa um indicador de pOH, por exemplo; quase sempre se pede o pH e pronto (ok, ok, são facilmente convertidos...). E definitivamente nunca usamos “básico” ou “alcalino” para denotar o sabor de uma fruta; por exemplo, dizemos que está “azeda” ou “ácida” ou mesmo “passada”. O uso da palavra “base” sempre esteve, portanto, à margem da moda, na Química, na Gastronomia ou na Literatura (Moreno, 2015).
Nas línguas anglo-saxônicas e latinas, a palavra “base” é um adjetivo pejorativo, herdado da corruptibilidade dos metais menos nobres. Um bom exemplo pode ser extraído da peça Otelo [II, ϭ], de Shakespeare (em inglês arcaico):
If thou be'st valiant,— as, they say, base men being in love have then a nobility in their natures more is native to them (em tradução livre: “Se vocês meus mais valentes, – como, eles dizem, homens vis estando apaixonados, têm então uma nobreza em sua natureza mais do que natural”).
É quando a Química se une à Literatura.
R. O cálculo está correto; a quantidade de matéria em 1 mol de qualquer substância é absurdamente grande, superior à quantidade de estrelas no Universo, estimada na assombrosa quantia de 70.000.000.000.000.000.000.000 estrelas, ou 7 x 1022. E 1 mol de água, por exemplo, não ocupa mais que a altura de um dedo em um copo comum de plástico (300mL). Não seria romântico contar para o seu namorado ou namorada, com um copo d’água na mão, que ali há mais moléculas do que a quantidade de estrelas que há em todo universo? Bom, pode não surtir muito efeito, entretanto é uma pequena demonstração da riqueza e grandiosidade do mundo microscópico da Química. Vejamos outras analogias:
Diante de tanta imensidão, o famoso verso do poeta inglês William Blake (1759-1827) faz pleno sentido:
Ver o Universo no grão de areia
e o Paraíso em uma flor;
segurar o Infinito na palma de sua mão
e notar a Eternidade em uma hora.
R. Claro que não, mas se eu tivesse uma banda de rock, chamaria de “radicais livres”! Seria um sucesso arrebatador!
Agora falando sério: os radicais livres são átomos, moléculas ou íons que possuem pelo menos um elétron da camada de valência desemparelhado, o que os torna extremamente reativos. São produzidos por diversos mecanismos; na verdade, sua presença é muito comum como intermediários das reações químicas, especialmente em altas temperaturas, como na combustão. Contudo, eles quase sempre não aparecem quando vemos uma equação balanceada; é como se os produtos tivessem surgido dos reagentes a partir de um passe de mágica. Nada mais desonesto para com os nossos radicais!
Os radicais livres ganharam fama nas últimas décadas a partir da descoberta de seu papel causador do envelhecimento, além de responsável pelo aparecimento de uma série de doenças, como câncer, AVC, enfarte do miocárdio, diabetes, aterosclerosis, esquizofrenia e Alzheimer. Como os radicais fazem parte dos mecanismos de reações necessárias para o funcionamento de qualquer organismo vivo, não há como impedir que ocorram; contudo, há como reduzir o seu efeito ou até reverter o seu dano. O consumo de vitaminas A, C e E, por exemplo, tem especial efeito benfazejo, são chamados de antioxidantes. A adoção de uma alimentação mais saudável e a prática regular de esportes é outra ideia radical.
R. Essa pergunta, que dá título a este artigo, é uma das principais causas de inquietação entre os químicos. Antes de explicarmos, já percebeu que há gafes na percepção popular para cada campo da ciência? Se quiser consternar um astrônomo, diga-lhe que as estrelas piscam no céu ou conte-lhe sobre o seu enorme apreço pela astrologia. Para provocar um biólogo, mencione que o macaco é ancestral do ser humano ou que a aranha é um inseto. Ou conte para um engenheiro que viu um motor movido a água ou, para um físico, que o spin do elétron representa a sua rotação ou, a pior de todas: que comprou um sal quântico para tratar a artrite de sua avó. Para provocar a inteligência de um químico, diga-lhe que um alimento ou um cosmético “não tem química”.
A noção popular de Química é bastante distinta da acadêmica. Para os químicos, toda matéria tem química, seja em um pulsar em uma galáxia distante ou na cera no ouvido de um camundongo. No saber comum, no entanto, a palavra “Química” está quase sempre associada a produtos nocivos para a saúde e para o ambiente, como agrotóxicos ou quaisquer aditivos cuja procedência ou natureza não esteja clara. Se tem algum potencial de fazer mal ao organismo, é porque “tem química”. É uma luta quixotesca tentar mudar esse imaginário depreciativo. Despejei parte de minha indignação nesta crônica (Moreno, 2018).
Se há algo que aparenta “não possuir química” é a antimatéria. Ela parece ser algo que não existe, não obstante tenha sido produzida em boas quantidades dentro de laboratórios do mundo inteiro. A antimatéria possui propriedades semelhantes à matéria; contudo, se ambas entrarem em contato, serão mutuamente aniquiladas, resultando apenas em luz de alta energia (raios gama). Apesar do nome, a antimatéria possui “matéria”; ela tem massa idêntica à de sua partícula correspondente, mas com carga elétrica invertida. Na verdade, há muita química na antimatéria: ela é aparentemente análoga à matéria. Recentemente, em nosso pequeno planeta, foi possível criar diversos átomos de anti-hidrogênio. Eles são feitos de antielétrons, mais conhecidos como pósitrons, circulando um antipróton, igual ao próton, mas com carga negativa.
Já há muito tempo que se especula uma realidade formada apenas por antimatéria. Quantidades iguais de matéria e antimatéria podem ter sido criadas logo após o Big Bang. Universos paralelos poderiam, a rigor, ser compostos de antimatéria e ser bastante similares ao nosso. É maravilhoso imaginar um mundo no qual formas alternativas de nossos corpos feitos de antimatéria poderiam conviver normalmente, interagindo uma com a outra sem se desintegrar. Como seria a vida de seu outro “eu” nesse outro universo? Estaria torcendo para um time de futebol ou algum candidato oposto ao seu preferido neste universo? Não existe qualquer limitação física para que isso ocorra; difícil é imaginar como acessaríamos esse mundo. Para quem aprecia o universo nerd, como eu, esse contexto foi explorado em uma das principais sagas dos quadrinhos da DC Comics, a Crise nas infinitas terras.
R. Na pele rola uma interação entre as moléculas de queratina da epiderme e demais substâncias que compõem a nossa superfície, como água, compostos orgânicos, sais minerais etc. Deve ter um pouco de tudo, dipolo-dipolo, dipolo-induzido, íon-dipolo, ligação de hidrogênio; até a gravidade ajuda.
R. Aí é pegar pesado com os gracejos... O poço de Lennard-Jones é uma medida das forças da interação entre duas partículas (Figura 1). A parte mais baixa do gráfico, o chamado poço de Lennard-Jones, denota a região de maior estabilidade, onde as forças de repulsão e atração encontram o melhor equilíbrio. Pode ser uma boa metáfora para as relações, nas quais deve existir um equilíbrio entre proximidade e distanciamento. (um quarto de século atrás meu professor usou esse exemplo). Definitivamente, não é uma boa metáfora para depressão. O fundo do poço é, na verdade, o lugar do equilíbrio, do encontro.
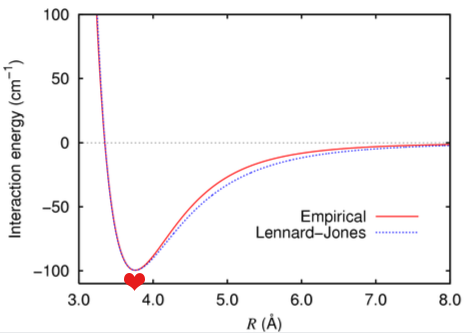
Figura 1. Diagrama de Lennard-Jones: representação do comportamento de interação energética entre duas partículas carregadas
Coube a Empédocles de Agrigento (492-432 a.C), um dos pré-socráticos mais brilhantes, a primeira associação entre as forças atrativas e repulsivas a sentimentos, respectivamente de amor e ódio. Ele postula que essas duas forças, de atração e repulsão, são responsáveis pela formação e organização de todo o universo, revezando de intensidade. Amor e ódio seriam, portanto, realidades naturais, participando de todas as interações da natureza. Os elementos que a compõem – i.e., terra, fogo, ar e água – fazem parte dessa dança de união e geração de combinações; ou destruição e afastamento, o que os conduziria à morte. Os elementos, contudo, permanecem inalterados, uma relação perfeitamente análoga aos nossos átomos.
R. Uma das origens da palavra Química deriva da palavra árabe “alquimia”, que por sua vez origina-se da palavra “chem”, que era um dos nomes do Egito antigo. Mas não é apenas um nome próprio: significa “terra negra” ou “terra escura”; na verdade, denota a riqueza mineral e de vida das terras que compunham os ricos solos às margens do Rio Nilo, que serviam com magnitude e realeza àquela grande civilização antiga (Alfonso-Goldfarb, 1987). Uma das principais origens da palavra Química, portanto, reflete uma fonte de abundância, significado que é geralmente esquecido pelos livros e, como consequência, parte de nossa herança imaginária da Química é pouco valorizada ou desconhecida.
Para ativar essa lembrança, o escritor, neurologista e químico amador Oliver Sacks (1933-2015) sintetizou o seu fascínio pela Química em seu livro de memórias, Tio Tungstênio, com esta preciosa frase (Sacks, 2002):
A Química tem talvez a mais intrincada, mais fascinante e, certamente, a mais romântica história entre todas as Ciências.
Se o Rio Tietê perpassa riqueza semelhante em nosso imaginário, o uso sugerido na pergunta é, grosso modo, apropriado, com o adicional de que a Química tem sido associada a poluição, que é uma das características mais denunciadas contra esse rico e famoso rio, especialmente enquanto atravessa a capital paulista.
R. Essa é a pergunta mais séria desta coleção e não se relaciona a algo trivial, pois não costuma ser explicada nos livros de Físico-Química. Mas a resposta é simples: a constante universal de “gases” (R) recebe esse nome por que foi originalmente descoberta em cálculos envolvendo gases; não obstante, posteriormente, observou-se que ela tem um significado ainda mais universal, a exemplo do que ocorre com a constante gravitacional (G) ou a constante de atração eletromagnética (K), entre muitas outras.
Podemos, neste caso, com a devida licença poética, associar a constante R a uma anacrese. Trata-se de uma figura de linguagem, um tipo particular de metáfora, que adquiriu maiores significados. É como o exemplo clássico da palavra "azulejo", que originalmente servia para designar ladrilhos azuis e passou a associar-se a ladrilhos de quaisquer cores.
R. Sim, é verdade, apesar de o gracejo poder parecer desagradável para alguns. Entretanto, do ponto de vista puramente químico, uma molécula gasosa não muda a sua identidade ou carrega memórias de onde tenha passado. Pode ocorrer, o que não é incomum, que ela reaja e forme outras moléculas, mas seus átomos manterão a mesma característica, assim como as suas subpartículas.
A reciclagem de átomos e moléculas na natureza é um capítulo especial da Biogeoquímica, estudado por meio de ciclos, como os de carbono, nitrogênio, ferro, oxigênio etc. Um importante corolário é que todos nós estamos intrinsecamente relacionados quimicamente, seja no reino mineral, vegetal, animal ou humano, seja na terra, nos oceanos, no ar ou mesmo no espaço, de onde, aliás, vieram todos os nossos átomos.
R. Anitta (lê-se anitxá) é o termo que descreve a máxima budista de que todos os fenômenos são impermanentes, isso é, qualquer "objeto" ou "experiência" deve mudar com o tempo, só existindo a partir de condições temporárias. Nada mais contraditório com o diamante, um dos símbolos mais recorrentes da permanência, tanto que desejamos e dispensamos um precioso soldo para presenteá-lo como representante da eternidade. Mas vamos desconstruí-lo aos poucos.
Excetuando as impurezas, o diamante tem a mesma composição que o carvão; ambos são constituídos de carbono e, portanto, podem ser queimados em presença de oxigênio. Como é um experimento muito caro, você não vai ver um químico torrando diamantes em seu laboratório; entretanto, desde o século XVIII ele tem sido queimado sob uma chama forte. A primazia de produzir CO2 e água a partir da combustão da preciosa gema coube a Antoine Lavoisier, que, além de um prodigioso químico, tinha fartos recursos financeiros. Logo comprovou que o carbono que compõe o diamante é o mesmo que compõe o carvão. Mas por que são tão diferentes?
A explicação é bem conhecida: está na forma como os átomos de carbono se unem em suas estruturas; o que poucos sabem é que o carvão é mais estável termodinamicamente que o diamante. Isso quer dizer que ele possui um arranjo atômico mais favorável a não se transformar em outra coisa. Como todas as transformações direcionam-se espontaneamente para o seu estado de maior estabilidade, o carvão, o mesmo usado na churrasqueira, tem maior sentido de receber o título de eterno do que o próprio diamante.
Por isso, pelo critério temporal, sim, faz mais sentido usar um pedaço de carvão em uma joia do que o rico e bem afamado diamante. Isso não quer dizer que, ao colocá-lo ao relento, ele irá permanecer da mesma forma que o diamante; mas, em condições controladas e estáveis, o nosso carvão tem maior estabilidade. Contudo, pensando bem, as rochas e as gemas, em geral, possuem um tempo de vida muito maior do que a existência humana, de forma que não faz muito sentido dizer que o diamante, o carvão, o rubi ou um silicato qualquer são eternos. Aliás, qual o tempo da eternidade? Grosso modo, toda essa “eternidade” será deglutida pelo Sol daqui a cerca de cinco bilhões de anos, quando nossa principal estrela virará uma gigante vermelha e, em sua expansão, fagocitará o nosso pequeno planeta.
Na verdade, é senso comum que o nosso apreço especial pelo diamante deu-se em grande parte pelo poderoso lobby da De Beers, multinacional que comercializava mais de 90% dos diamantes do mundo. Para termos uma dimensão de seu poder, quando a antiga União Soviética entrou em crise, ela colocou à venda toda a sua reserva de diamantes, estimada na época em US$ 3 bilhões. A De Beers comprou tudo e, dessa forma, manteve o elevado preço dessa gema nos mercados mundiais. Durante a década de 1970, ela chegou a financiar secretamente o filme Os diamantes são eternos, da série 007. Nós caímos nessa, né?!
Aliás, você já se perguntou por que precisamos, como prova de amor, presentear (ou sacrificar o nosso apertado orçamento) com algo eterno? Nem mesmo todas as gerações de vida na Terra poderiam ou poderão alcançar essa prerrogativa. “Que seja eterno”, como dizia o poetinha, “enquanto dure”, ou, na poesia de Paulo Leminski:
Dura o diamante
dentro da pedra dura
de agora em diante
só o durante dura.
E, se ainda assim quisermos insistir em adquirir a eternidade por meio de um diamante, há empresas especializadas em transformar nossos entes queridos ou até o nosso amado pet em uma linda joia que pode ser pendurada no pescoço, separando a cabeça do resto do corpo e do resto de tudo.
Seguem mais 5 perguntinhas bônus para curtir e colecionar! ;-)
- Se o lixo é orgânico, por que não podemos depositar-lhe restos de plásticos e papelão?
- Um veneno com o prazo de validade vencido é mais tóxico ou menos tóxico?
- Se o humor pode ser ácido, o mau humor pode ser básico?
- Se a bolacha é de água e sal, quer dizer que ela foi produzida a partir da reação de um ácido com uma base?
- Se um átomo de hidrogênio tem cerca de 10-10 metro, ou 0,0000000001 metro, qual o tamanho da régua que o mediu?
Referências
ALFONSO-GOLDFARB, A. M. Da Alquimia à Química. São Paulo: Nova Stela/Edusp, 1987.
ELIADE, M. Ferreiros e alquimistas. Rio de Janeiro: Zahar, 1979.
MORENO, E. L. Como matar um químico. Revista Educação Pública, Rio de Janeiro, v. 19, nº 9, 8 de maio de 2018. Disponível em: https://educacaopublica.cecierj.edu.br/artigos/18/9/como-matar-um-quimico
______; MARTINS, E.; RAJAGOPAL, K. Basicidade e acidez, da Pré-História aos dias atuais. Rev. Virtual Quim, v. 7(3), p. 893-902, 2015. Doi: 10.5935/1984-6835.20150046.
SACKS, Oliver. Tio Tungstênio. São Paulo: Companhia das Letras, 2002.
Publicado em 11 de outubro de 2022
Como citar este artigo (ABNT)
MORENO, Esteban Lopez. Cosméticos e alimentos “sem química” são feitos de antimatéria? Revista Educação Pública, Rio de Janeiro, v. 22, nº 38, 11 de outubro de 2022. Disponível em: https://educacaopublica.cecierj.edu.br/artigos/22/38/cosmeticos-e-alimentos-rsem-quimicar-sao-feitos-de-antimateria
Novidades por e-mail
Para receber nossas atualizações semanais, basta você se inscrever em nosso mailing
Este artigo ainda não recebeu nenhum comentário
Deixe seu comentárioEste artigo e os seus comentários não refletem necessariamente a opinião da revista Educação Pública ou da Fundação Cecierj.

